Una vacuna diseñada para combatir los cánceres de cabeza y cuello provocados por el VPH ha mostrado resultados prometedores en un estudio de laboratorio en tejidos humanos y ratones Si se demuestra su eficacia en humanos, la inyección terapéutica podría complementar las terapias estándar contra el cáncer, y su diseño puede ayudar a los científicos a construir mejores vacunas para otras enfermedades.
El virus del papiloma humano (VPH), causante de la mayoría de los casos de cáncer de cuello uterino, también causa otros tipos de cáncer, como el cáncer orofaríngeo (cáncer de garganta). En Estados Unidos, aproximadamente el 70% de los cánceres orofaríngeos están relacionados con el VPH. Si bien existen más de 100 cepas de VPH, sólo 12 se consideran de alto riesgo; casi todos los casos de cáncer de garganta relacionado con el VPH son causados por la cepa de alto riesgo 16.
La vacuna Gardasil 9 puede prevenir las infecciones por VPH y, por lo tanto, reducir el riesgo de estos cánceres en el futuro. Sin embargo, para las personas que ya tienen tumores relacionados con el VPH, el tratamiento aún se basa en cirugía, radioterapia y quimioterapia. Combinar una vacuna contra el cáncer con estas terapias convencionales podría aumentar su eficacia al enseñar al sistema inmunitario a combatir el cáncer.
Ahora, científicos han diseñado una vacuna contra el cáncer cuyos componentes están dispuestos en una estructura única. Al igual que las vacunas preventivas, las vacunas contra el cáncer entrenan al sistema inmunitario para reconocer proteínas específicas —en este caso, una proteína presente en tumores VPH positivos— y suelen contener ingredientes llamados adyuvantes que estimulan la respuesta inmunitaria. Sin embargo, en lugar de prevenir la enfermedad desde el principio, las vacunas contra el cáncer se utilizan generalmente para tratarla y ayudar a prevenir su recurrencia.
En estudios de laboratorio sobre cáncer de cabeza y cuello con VPH positivo, esta nueva vacuna cuidadosamente diseñada desaceleró el crecimiento del tumor y mejoró la supervivencia en ratones, según un estudio publicado el miércoles 11 de febrero en la revista Science Advances. El Dr. Ezra Cohen, especialista en cáncer de cabeza y cuello de UC San Diego Health, que no participó en el estudio, dijo que si la vacuna funciona en humanos, podría complementar las terapias estándar.
“Se puede imaginar un enfoque multimodal para que un paciente se cure de la enfermedad y luego la vacuna para prevenir la recurrencia”, dijo. Sin embargo, advirtió que los resultados en animales de laboratorio y tejidos aislados no siempre se aplican a los humanos. “La verdadera prueba está en las personas”, declaró a Live Science en un correo electrónico. “Pero datos preclínicos sólidos, como estos, aumentan las probabilidades de éxito en los ensayos clínicos”.
En este caso, lo que llama la atención es el diseño subyacente de la vacuna.
“El hallazgo clave es que la estructura de la vacuna marca una diferencia significativa”, afirmó Cohen. “El éxito de la vacunación no se limita a seleccionar los antígenos correctos [proteínas diana], sino a colocarlos en la secuencia correcta con otros elementos de la vacuna”.
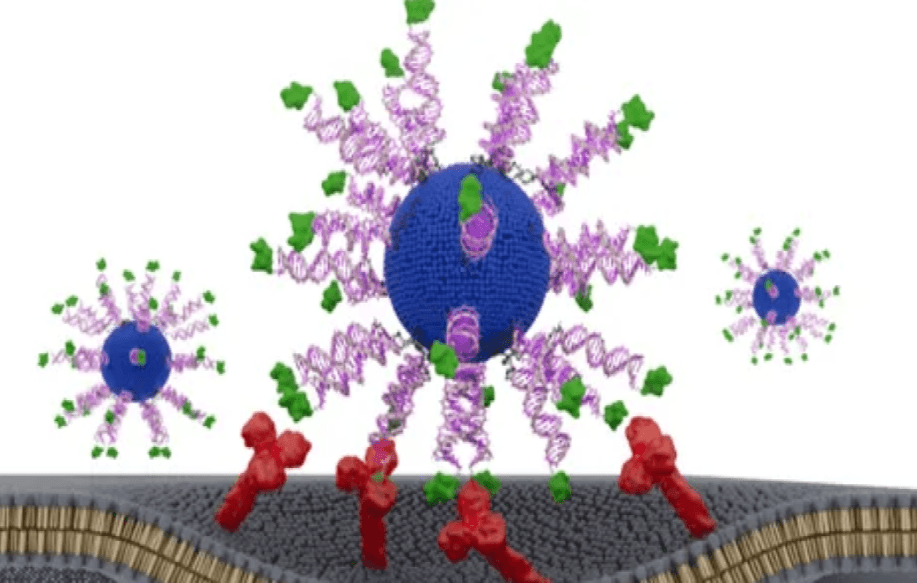
La vacuna utiliza ácidos nucleicos esféricos (SNA), partículas de ADN con forma de globo que penetran en las células inmunitarias y se unen a sus dianas con mayor eficacia que el ADN lineal. Cada nanopartícula de SNA de la vacuna consiste en un núcleo graso rodeado de un adyuvante y un fragmento de una proteína del VPH procedente de las células tumorales. El adyuvante imita el ADN bacteriano y es reconocido por el sistema inmunitario como “extraño”.
Los investigadores probaron tres diseños, modificando únicamente la posición del fragmento de VPH. Una versión lo ocultaba dentro de la nanopartícula, mientras que las otras dos versiones lo tenían en la superficie de la partícula, adherido a diferentes extremos de la estructura, conocidos como el extremo N y el extremo C.
El equipo descubrió que la versión con el fragmento adherido a la superficie a través de su extremo N-terminal desencadenó la respuesta inmunitaria más potente. Este diseño provocó que los linfocitos T citotóxicos (células inmunitarias que destruyen las células infectadas, dañadas y cancerosas) produjeran hasta ocho veces más interferón gamma, una proteína clave de señalización antitumoral. Esto los hizo más eficaces para eliminar las células cancerosas positivas al VPH.
En modelos murinos de cáncer con VPH positivo, la vacuna ralentizó significativamente el crecimiento tumoral. Además, al probarse en muestras tumorales de pacientes con cáncer con VPH positivo, la vacuna con extremo N-terminal destruyó de dos a tres veces más células cancerosas que los otros dos diseños de vacuna.
“Este efecto no se produjo al agregar nuevos ingredientes ni al aumentar la dosis. Se produjo al presentar los mismos componentes de una manera más inteligente”, afirmó en un comunicado el Dr. Jochen Lorch, coautor del estudio y director de oncología médica del Programa de Cáncer de Cabeza y Cuello de Northwestern Medicine.
“El sistema inmunitario es sensible a la geometría de las moléculas”, afirmó. “Al optimizar la unión del antígeno al SNA, las células inmunitarias lo procesaron con mayor eficiencia”.
De cara al futuro, el coautor del estudio, Chad Mirkin, inventor de los SNA y director del Instituto Internacional de Nanotecnología de Northwestern, espera que este enfoque pueda ayudar a los científicos a rediseñar vacunas más antiguas que inicialmente parecían prometedoras pero fracasaron.
“Este enfoque está llamado a cambiar la forma en que formulamos las vacunas”, declaró Mirkin. “Es posible que hayamos descartado componentes de vacunas perfectamente aceptables simplemente porque estaban en configuraciones incorrectas. Podemos retomarlos, reestructurarlos y transformarlos en medicamentos potentes”.
Fuente: Live Science.