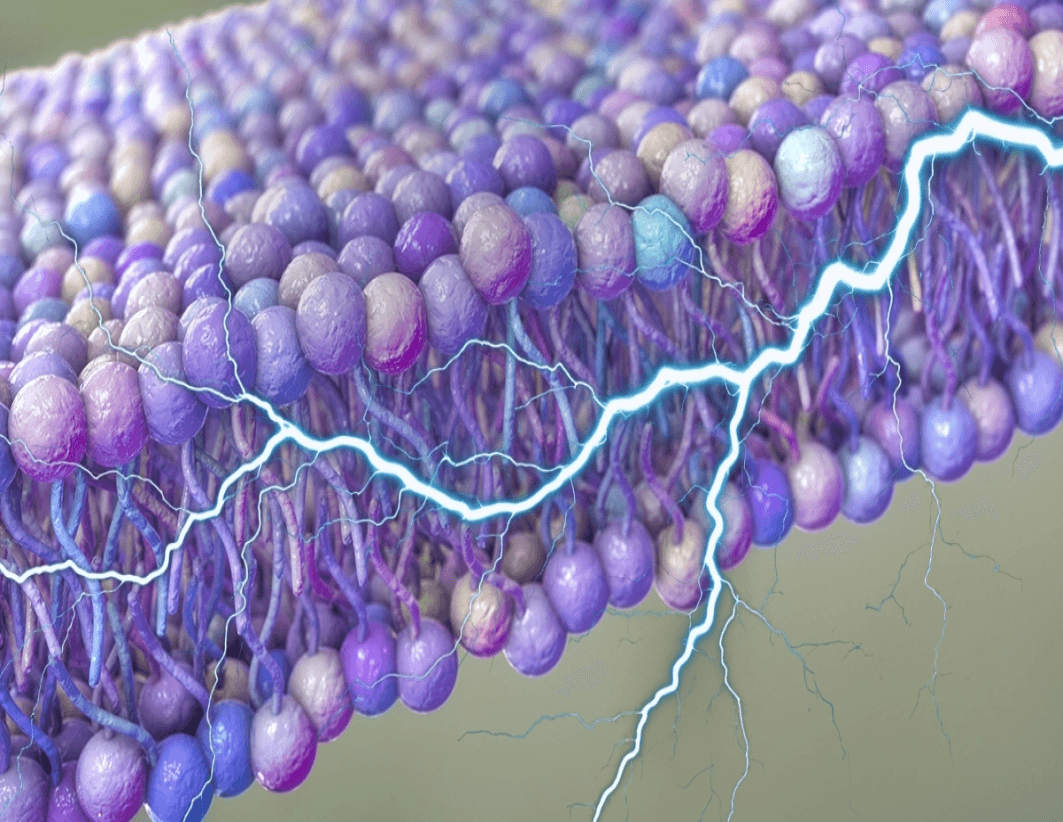
Nuestras células pueden literalmente ondularse con electricidad, actuando como una fuente de energía oculta que podría ayudar a transportar materiales o incluso desempeñar un papel en la comunicación de nuestro cuerpo. Investigadores de la Universidad de Houston y la Universidad Rutgers en EE.UU. sugieren que pequeñas ondas en las membranas grasas que rodean nuestras células podrían generar suficiente voltaje para servir como fuente directa de energía para algunos procesos biológicos.
Las fluctuaciones en sí mismas ya han sido ampliamente estudiadas y se sabe que son impulsadas por la actividad de las proteínas incrustadas y la descomposición del adenosín trifosfato (ATP), el principal medio de transporte de energía a través de las células. El nuevo estudio proporciona apoyo teórico a la posibilidad de que los movimientos de la membrana sean lo suficientemente fuertes y estructurados como para crear una carga eléctrica que las células puedan utilizar para algunas tareas importantes.
“Las células no son sistemas pasivos: están impulsadas por procesos internos activos, como la actividad proteica y el consumo de ATP”, escriben los investigadores en su artículo publicado.
“Demostramos que estas fluctuaciones activas, cuando se combinan con la propiedad electromecánica universal de la flexoelectricidad, pueden generar voltajes transmembrana e incluso impulsar el transporte de iones”.
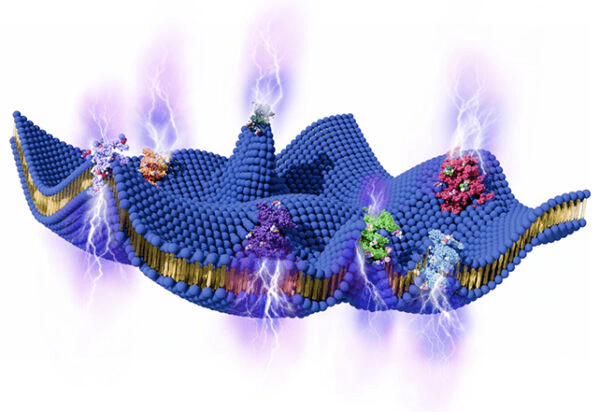
La clave para entender el nuevo modelo es el concepto de flexoelectricidad, que describe esencialmente los medios por los cuales se puede producir un voltaje entre puntos contrastantes de tensión en un material. Las membranas se doblan constantemente debido a las fluctuaciones aleatorias del calor a través de la célula. En teoría, cualquier voltaje producido de esta manera debería cancelarse en entornos en equilibrio, lo que las hace inservibles como fuentes de energía.
Los investigadores razonaron que las células no están en estricto equilibrio, y que la actividad en su interior se concentra en mantenernos vivos. Para determinar si esto sería suficiente para convertir una membrana lipídica en un motor, se requerían algunas formulaciones detalladas.
Según los cálculos realizados por los investigadores, la flexoelectricidad podría crear una diferencia eléctrica entre el interior y el exterior de la célula: hasta 90 milivoltios, que es suficiente carga para que una neurona se active.
El voltaje producido podría ayudar en el movimiento de iones, los átomos cargados que son controlados por el flujo de electricidad y productos químicos. Las fluctuaciones de la membrana podrían ser suficientes para influir en funciones biológicas como el movimiento muscular y las señales sensoriales. El equipo estimó que las cargas surgen en una escala de milisegundos, lo que coincide con la sincronización de las señales que recorren las neuronas.
“Nuestros resultados revelan que la actividad puede amplificar significativamente el voltaje transmembrana y la polarización, lo que sugiere un mecanismo físico para la recolección de energía y el transporte dirigido de iones en células vivas”, escriben los investigadores.
Los hallazgos también podrían extenderse a otros grupos celulares, ayudando a explicar cómo se coordinan las membranas celulares para generar efectos y tejidos a mayor escala. Estudios futuros podrán comprobar si todo esto funciona correctamente dentro del cuerpo.
Estos hallazgos podrían tener implicaciones más allá de los tejidos vivos: los investigadores plantean la idea de utilizar estas mismas técnicas de producción de electricidad para informar el diseño de redes de inteligencia artificial y materiales sintéticos basados en la naturaleza.
“Investigar la dinámica electromecánica en redes neuronales puede unir la flexoelectricidad molecular y el procesamiento de información compleja, con implicaciones tanto para la comprensión de la función cerebral como para el descubrimiento de materiales computacionales bioinspirados”, escriben los investigadores.
La investigación ha sido publicada en PNAS Nexus.
Fuente: Science Alert.