Los patógenos causantes de enfermedades son enemigos notoriamente peligrosos que han desarrollado muchos trucos para frustrar el sistema inmunológico del cuerpo. Entre los más terroríficos están los que pueden colarse en el sistema nervioso, llegando incluso a infectar el cerebro.
Ahora, un nuevo estudio de investigadores del Reino Unido, Australia y Singapur capturó un lapso de tiempo de destrucción en el pez cebra cultivado en laboratorio, mostrando cómo un hongo que causa un tipo raro de meningitis se propaga fuera del torrente sanguíneo y hacia el cerebro. Como si pasar entre las células apretadas de la barrera hematoencefálica o hacer autostop dentro de las células inmunitarias destinadas al cerebro (como hacen muchos otros patógenos) no fuera suficiente, parece que un microbio causante de la meningitis que se conoce con el nombre de Cryptococcus neoformans tiene otro as bajo la manga: bloquear y reventar pequeños vasos sanguíneos en el cerebro del pez cebra.
“El cerebro tiene defensas muy complejas y efectivas contra los microbios”, dice el autor principal Simon Johnston, investigador de enfermedades infecciosas de la Universidad de Sheffield, Reino Unido.
“Pero hemos identificado un método simple y efectivo que los microbios pueden usar para escapar de la sangre y entrar al cerebro”.
La meningitis es una enfermedad potencialmente mortal causada por infecciones bacterianas o fúngicas del cerebro y la médula espinal que provocan hinchazón e inflamación de las meninges, la membrana protectora que recubre el sistema nervioso central. La meningitis puede ser fatal si no se reconoce y trata rápidamente; un problema que empeora por la creciente amenaza de infecciones resistentes a los antimicrobianos, que ahora son la tercera causa de muerte en todo el mundo. Los receptores de trasplantes de órganos, las personas con VIH/SIDA y otras personas con sistemas inmunitarios debilitados corren mayor riesgo de contraer meningitis fúngica, que no se propaga directamente entre las personas y solo se puede contraer del medio ambiente.
Si bien puede haber muchos culpables microscópicos de la meningitis, muchos de los cuales se encuentran en suelos llenos de insectos, C. neoformans causa meningitis fúngica, que es más rara que otras formas de la enfermedad que se pueden prevenir con la vacunación. Se sabe que el patógeno daña los vasos sanguíneos, pero no está claro exactamente cómo.
“Comenzamos esta investigación porque sabíamos que había un daño inexplicable en los vasos sanguíneos en algunos pacientes con meningitis”, dice Johnston, quien en trabajos anteriores expuso cómo C. neoformans manipula las células inmunitarias.
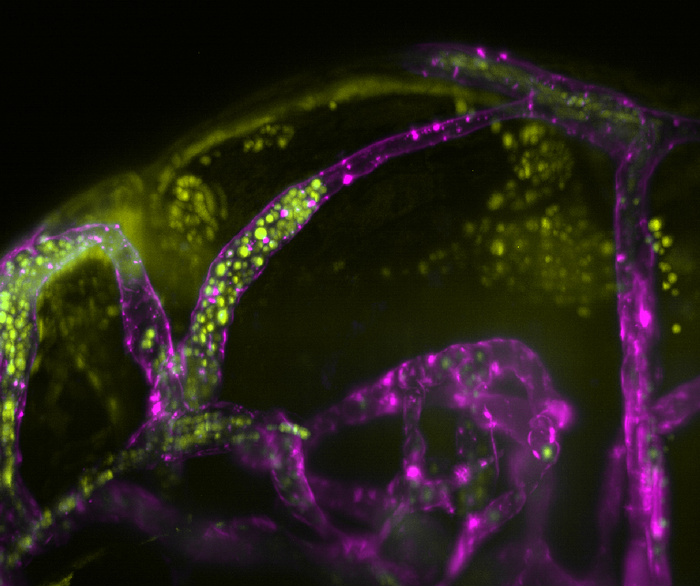
En este estudio, Johnston y sus colegas utilizaron peces cebra transparentes de rápido crecimiento para observar cómo se comporta C. neoformans en los vasos sanguíneos, que están teñidos de púrpura en la imagen a continuación. Las esporas del hongo C. neoformans se representan en amarillo fluorescente.
Utilizando técnicas de imágenes de células vivas de alta resolución, los investigadores visualizaron los invasores fúngicos transmitidos por la sangre marcados con fluorescencia durante varios días. Los microbios se alojaron en los vasos sanguíneos, restringiendo el flujo sanguíneo y bloqueando el suministro de sangre. A medida que los microbios infecciosos se multiplicaron, los vasos sanguíneos se estiraron y se rompieron, liberando C. neoformans en el tejido cerebral del pez cebra.
Incluso las células individuales de C. neoformans podrían encajar en pequeños vasos sanguíneos, sembrando masas fúngicas que bloquean los vasos sanguíneos. Estas se parecían inquietantemente a las masas fúngicas o bacterianas que se encuentran junto a los capilares cerebrales en los informes post-mortem de personas que habían muerto a causa de la enfermedad. En el pez cebra, los bloqueos no solo aumentaron la presión arterial local, sino que, a medida que el flujo sanguíneo retrocedió, la obstrucción fúngica también aumentó la tensión de las paredes de los vasos sanguíneos cercanos, haciéndolos más propensos a romperse.
“La investigación anterior se ha centrado en cómo los microbios pueden romper las defensas del cerebro o utilizar las células inmunitarias como ruta hacia el cerebro”, dice Johnston. “Podemos demostrar cómo, para algunos microbios, dañar los vasos sanguíneos es un método de invasión muy efectivo”.
Además de eso, y esto es muy esclarecedor, el equipo también descubrió que las masas de C. neoformans se acumularon en promedio dos días antes de que los vasos sanguíneos estallaran, una ventana estrecha en la que los médicos posiblemente podrían intervenir para detener una infección antes de que se produzca el daño.
“Las infecciones que causan meningitis se pueden tratar con antimicrobianos, pero los pacientes a menudo están muy enfermos y se pueden causar muchos daños antes de que el tratamiento sea efectivo”, dice Johnston.
Con suerte, comprender cómo se propaga la meningitis fúngica en el cerebro conducirá a nuevas terapias que ayuden a limitar el daño a los vasos sanguíneos del cerebro, mientras que los tratamientos antimicóticos funcionan para eliminar la infección. Cualquier tratamiento de este tipo es solo una quimera en esta etapa, ya que los experimentos de imágenes se realizaron en diminutos peces cebra. Sin embargo, Johnston y sus colegas creen que sus hallazgos podrían ser relevantes para otros tipos de infecciones que dañan o rompen los vasos sanguíneos, aunque señalan que estos mecanismos probablemente varíen entre las especies microbianas.
El estudio fue publicado en PLOS Pathogens.
Fuente: Science Alert.