Los científicos han desarrollado un método para convertir las propias células inmunitarias del cuerpo en agentes anticancerígenos —sin extraerlas del organismo— utilizando glóbulos rojos para transmitir instrucciones genéticas. Las terapias CAR (receptor de antígeno quimérico) actuales suelen implicar la extracción de linfocitos T del paciente, su modificación genética en el laboratorio y su posterior reinfusión, un proceso que puede durar semanas. La nueva estrategia busca evitar este paso.
En un estudio publicado en Science Translational Medicine, investigadores del Laboratorio Westlake de Ciencias de la Vida y Biomedicina en Hangzhou, China, informan que utilizaron eritrocitos modificados genéticamente, o glóbulos rojos, para transportar ARN mensajero (ARNm) que reprograma las células mieloides para convertirlas en células dirigidas contra tumores dentro del cuerpo.
“La ingeniería de células mieloides con receptores de antígenos quiméricos (CAR) ofrece grandes posibilidades terapéuticas”, escribe la Dra. Xiaoqian Nie, autora principal de la investigación.
“Hemos desarrollado una plataforma de administración de ARN mensajero mediada por eritrocitos, denominada mRNA-LNP-Ery, en la que nanopartículas lipídicas cargadas con ARNm se anclan covalentemente a los eritrocitos”.
Un cambio de las terapias celulares de laboratorio a las terapias celulares intracorporales
Este enfoque representa una nueva dirección potencial para la inmunoterapia contra el cáncer, evitando el complejo y costoso proceso de extracción y manipulación genética de células fuera del cuerpo. En cambio, los investigadores utilizaron glóbulos rojos como vehículos de administración para transportar directamente al organismo las construcciones de ARNm que codifican CAR. Una vez administradas, las instrucciones genéticas son captadas por las células mieloides, un tipo de células inmunitarias que incluye a los macrófagos, los cuales desempeñan un papel fundamental en el microambiente tumoral.
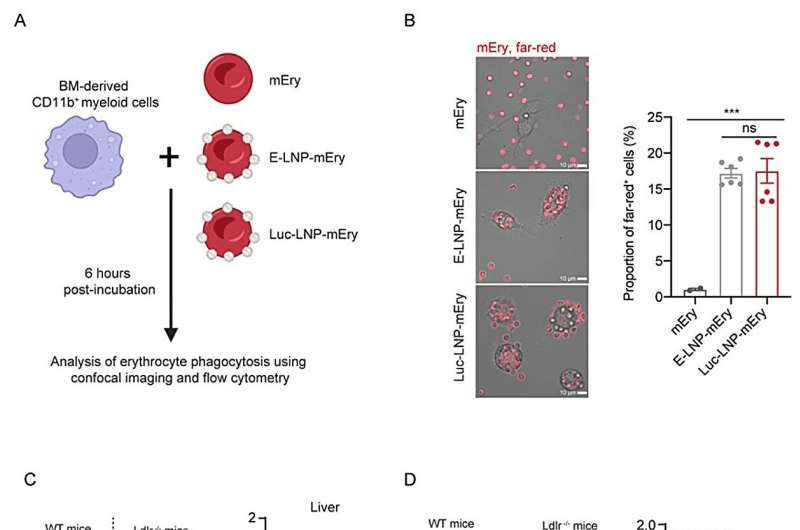
Tras recibir el ARNm, las células mieloides comenzaron a expresar moléculas CAR, receptores modificados genéticamente que permiten a las células inmunitarias reconocer y atacar las células cancerosas. A diferencia de las células CAR-T, que atacan principalmente el cáncer a través de mecanismos inmunitarios adaptativos, las células mieloides modificadas con CAR pueden infiltrarse en los tumores y remodelar el microambiente tumoral, superando potencialmente las barreras que limitan las terapias con células T.
En modelos animales preclínicos, las células mieloides CAR generadas in vivo mostraron actividad antitumoral, lo que sugiere que este enfoque puede reprogramar eficazmente las células inmunitarias donde se necesitan. Este método no hace que las terapias con células CAR-T queden obsoletas para el cáncer u otras afecciones médicas.
En un estudio publicado en enero, también en Science Translational Medicine, científicos de la Escuela de Medicina Icahn en Mount Sinai, en la ciudad de Nueva York, demostraron que las células T CAR producidas in vivo pueden atacar y eliminar las células del hígado que favorecen la fibrosis. La producción de células T CAR in vivo para tratar la fibrosis hepática podría resultar una terapia eficaz. Al igual que la investigación realizada en China, el estudio del Monte Sinaí utilizó un modelo animal preclínico.
¿Por qué los glóbulos rojos?
Mientras tanto, la investigación de Nie y sus colegas reveló que los glóbulos rojos ofrecen varias ventajas como vehículos de administración. Son abundantes, biocompatibles y circulan ampliamente por todo el cuerpo, lo que los convierte en una plataforma atractiva para distribuir moléculas terapéuticas.
Este nuevo enfoque también permite que los ARNm eludan las fuerzas de vigilancia inmunitaria en el bazo, que habían frenado intentos anteriores de generar células mieloides CAR in vivo. La terapia con células mieloides CAR se perfila como una herramienta prometedora para la inmunoterapia del cáncer, ya que las células mieloides CAR modificadas genéticamente pueden fagocitar células tumorales y amplificar otras respuestas inmunitarias antitumorales.
“Estas células migraron a los tumores, eliminaron las células cancerosas y remodelaron el microambiente tumoral, lo que provocó una mayor infiltración de linfocitos T efectores y células asesinas naturales”, escribió Nie en el estudio.
Al introducir ARNm en los eritrocitos, los investigadores crearon un sistema capaz de transmitir instrucciones genéticas sin desencadenar fuertes reacciones inmunitarias ni requerir vectores virales. En un resumen editorial de la investigación, la Dra. Amy E. Baek, editora asociada de Science Translational Medicine, escribió que la estrategia representa un nuevo método potencialmente eficaz para abordar el cáncer que, además, reduce la progresión del tumor y recluta la infiltración de células T y células asesinas naturales.
“Este trabajo proporciona un enfoque innovador para la generación in vivo de células efectoras CAR basadas en la línea mieloide”, escribió Baek.
Una nueva dirección para las terapias CAR
Los resultados apuntan a un posible cambio en la forma en que se desarrollan y administran las terapias basadas en células. Al generar células inmunitarias modificadas genéticamente directamente dentro del cuerpo, este enfoque podría simplificar la fabricación, reducir los costos y ampliar el acceso a tratamientos que actualmente están limitados a centros especializados.
Esta estrategia también abre la puerta a potenciar la capacidad de las células mieloides para combatir el cáncer, ya que estas células, cada vez más reconocidas como objetivos de las células tumorales, pueden manipular las células inmunitarias mieloides para que realicen actividades que favorezcan el crecimiento del cáncer y la inmunosupresión. Aunque el trabajo aún se encuentra en una etapa preclínica, sugiere que la programación in vivo de células inmunitarias podría complementar —o en algunos casos reemplazar— los enfoques tradicionales “ex vivo”.
Al combinar la administración de ARNm con el sistema de distribución natural de los glóbulos rojos, el estudio presenta una nueva forma de aprovechar el sistema inmunitario contra el cáncer. Si se sigue desarrollando, este enfoque podría ampliar el alcance de las terapias basadas en CAR más allá de las células T y acercar el tratamiento personalizado del cáncer a una realidad más escalable y disponible de forma inmediata.
“Nuestros hallazgos establecieron una plataforma de ARNm basada en eritrocitos con aplicabilidad clínica que permite la programación directa de células inmunitarias in vivo y promueve las terapias mieloides CAR para tumores sólidos”, concluyó Nie.
Fuente: Medical Xpress.