Hace casi un siglo, rumores de una maldición mortal rodearon al equipo que desenterró la tumba del rey Tutankamón. Uno tras otro, los arqueólogos que entraron en la tumba enfermaron o murieron en circunstancias misteriosas. Décadas más tarde, un grupo de investigadores polacos que excavaban la cripta del rey Casimiro IV corrió una suerte similar. Diez de los doce científicos fallecieron poco después de la exposición.
En aquel entonces, algunos pensadores más serenos especularon que el moho tóxico podría haber sido el culpable. Finalmente, esto se confirmó. Ahora, los científicos han vuelto a ese mismo hongo, Aspergillus flavus, no para temerlo, sino para aprovechar su poder.
Un nuevo estudio publicado en Nature Chemical Biology revela que este hongo mortal podría ser la fuente de un potente tratamiento contra el cáncer. Investigadores de la Universidad de Pensilvania y colaboradores de todo el mundo han convertido uno de los mohos más tóxicos conocidos por la ciencia en un prometedor compuesto antileucémico.
“Esta es la ironía de la naturaleza en su máxima expresión”, afirmó Sherry Gao, autora principal del estudio y profesora de ingeniería química y biomolecular en la Universidad de Pensilvania. “El mismo hongo que antes se temía por causar la muerte ahora podría salvar vidas”.
El hongo maldito
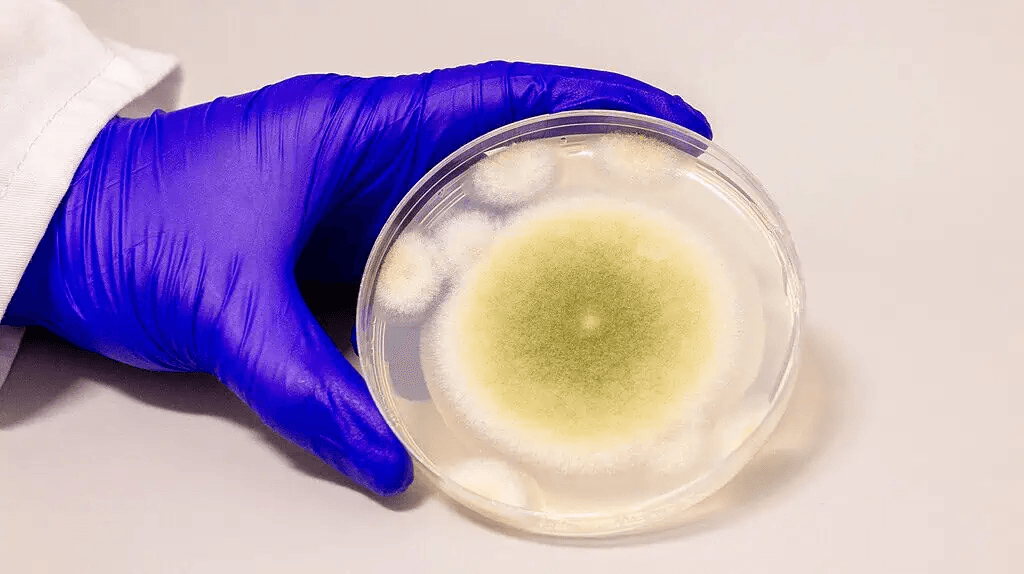
El Aspergillus flavus es un hongo común del suelo. Produce esporas amarillas resistentes y es conocido por contaminar cultivos y causar infecciones pulmonares, especialmente en personas con sistemas inmunitarios debilitados. Sin embargo, su siniestra reputación se vio cimentada por la llamada “maldición del faraón“.
Cuando Lord Carnarvon, quien financió la excavación del Rey Tut, falleció meses después de entrar en la tumba en 1922, se desató la especulación ¿Se trataría de superstición o de algo biológico?
En la década de 1970, la muerte de arqueólogos polacos que entraban en la tumba del rey Casimiro IV provocó un escrutinio más minucioso. Las pruebas encontraron A. flavus en la cámara funeraria. Al parecer, el hongo podía permanecer latente durante siglos, a la espera de liberar sus esporas al ser perturbado. Ahora, los científicos están volviendo a mirarlo.
De asesino a cura
El equipo de investigación buscaba una clase de moléculas conocidas como RiPP (péptidos sintetizados ribosómicamente y modificados postraduccionalmente). Se trata de pequeñas proteínas producidas en las células y modificadas químicamente posteriormente, a menudo mediante enzimas. Si bien se han encontrado miles de RiPP en bacterias, rara vez se observan en hongos.
“Purificar estas sustancias químicas es difícil”, explicó Qiuyue Nie, primera autora del estudio e investigadora postdoctoral en la Universidad de Pensilvania. “Pero eso también es lo que les confiere esta notable bioactividad”.
El equipo analizó una docena de cepas de hongos Aspergillus, comparando sus perfiles químicos con las estructuras conocidas de RiPP. Una cepa de A. flavus destacó. El análisis genético indicó una proteína que parecía clave para la producción de RiPP. Cuando los investigadores desactivaron el gen responsable de dicha proteína, los marcadores de RiPP desaparecieron.
Esto los condujo a una nueva clase de moléculas con una arquitectura compleja: anillos entrelazados construidos alrededor de un núcleo de benzofuranoindolina. Denominaron a estos compuestos “asperigimicinas”.
Incluso en su estado natural, algunas asperigimicinas destruyeron células leucémicas en pruebas de laboratorio. Pero los investigadores fueron más allá. Al añadir un ácido graso —similar a los lípidos presentes en la jalea real que alimenta a las abejas reinas—, potenciaron el poder anticancerígeno del compuesto. En pruebas comparativas, la versión mejorada, llamada 2-L6, funcionó tan bien como la citarabina y la daunorrubicina, dos medicamentos que han sido la piedra angular del tratamiento de la leucemia durante décadas.
“Un derivado con un ácido graso lineal C-11… alcanza una potencia anticancerígena nanomolar comparable a la de los fármacos antileucémicos clínicamente aprobados”, señala el estudio.
Huelga selectiva
Los investigadores también descubrieron algo inesperado: las asperigimicinas parecen actuar específicamente sobre las células leucémicas. Tuvieron poco o ningún efecto sobre las células cancerosas de mama, hígado o pulmón, ni sobre diversas bacterias y hongos.
Ese tipo de precisión es rara y muy, muy valiosa.
“Las células cancerosas se dividen sin control”, dijo Gao. “Estos compuestos bloquean la formación de microtúbulos, esenciales para la división celular”.
Al interrumpir este proceso sólo en las células de leucemia, los compuestos podrían ofrecer una manera de tratar el cáncer sin los amplios daños colaterales causados por muchas quimioterapias.
La farmacia oculta de hongos
El descubrimiento de las asperigimicinas es solo el comienzo. Utilizando los mismos métodos, los investigadores han identificado grupos de genes similares en otros hongos.
“Aunque solo se han encontrado unos pocos, casi todos presentan una fuerte bioactividad”, afirmó Nie. “Esta es una región inexplorada con un enorme potencial”.
El siguiente paso es probar los compuestos en modelos animales. Si estos ensayos tienen éxito, el equipo espera iniciar ensayos clínicos en humanos en el futuro.
Por ahora, A. flavus sigue siendo un peligro en cultivos alimentarios y tumbas polvorientas. Pero también nos recuerda que la naturaleza suele esconder sus mejores medicinas en los lugares más inesperados.
“La naturaleza nos ha dado esta increíble farmacia”, dijo Gao. “Depende de nosotros descubrir sus secretos”.
El estudio fue una iniciativa global que contó con la experiencia de la Universidad de Pensilvania, la Universidad Rice, el Centro Oncológico MD Anderson, la Universidad de Washington en San Luis, el Baylor College of Medicine, la Universidad de Pittsburgh y la Universidad de Porto. Fue financiado por los Institutos Nacionales de Salud, la Fundación Nacional de Ciencias y varias fundaciones e institutos de investigación del cáncer.
Fuente: ZME Science.

