Si bien los seres humanos poseemos impresionantes capacidades de autocuración, estamos muy lejos del nivel de las salamandras o los ajolotes, que pueden regenerar extremidades enteras; pero ¿podría eso cambiar en el futuro?
Un equipo liderado por investigadores de la Universidad de Texas A&M logró estimular con éxito la regeneración de tejido en ratones a los que se les había amputado un dedo del pie. Si bien la regeneración fue “imperfecta”, según informan los investigadores, los resultados son sin duda alentadores.
La técnica empleada aquí no ha sido probada en humanos, pero considerando las similitudes biológicas entre los mamíferos, resulta tentador pensar qué podrían hacer nuestras propias células, dadas las instrucciones adecuadas.
La clave del proceso residía en la aplicación de dos proteínas que emiten señales específicas: la primera genera la materia prima para la regeneración y la segunda construye tejido a partir de ella.
“En realidad, se trata de un proceso de dos pasos”, afirma Ken Muneoka, biólogo regenerativo de la Universidad de Texas A&M.
“Primero se desvían las células para evitar la formación de cicatrices, y luego se les proporcionan las señales que les indican qué deben construir”.
La formación de cicatrices es la reacción natural ante una lesión. Las células fibroblastos se dirigen al lugar de la herida para repararla con tejido cicatricial, una forma eficaz de detener la hemorragia, pero en el caso de una extremidad perdida, esta no se regenerará.
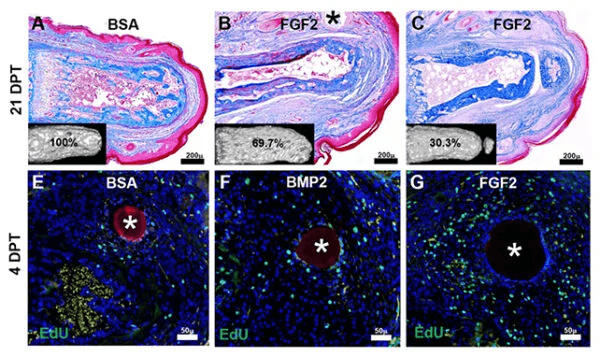
Estos fibroblastos se encuentran en un estado activo y receptivo mientras realizan su función, y es ahí donde entra en juego la primera proteína de señalización: el factor de crecimiento de fibroblastos 2 (FGF2). Básicamente, reprograma estas células, preparándolas para transformarse en otro tipo celular.
Ese otro tipo es un blastema. Se trata de “brotes” celulares temporales que utilizan animales como las salamandras para preparar el tejido para su regeneración, no sólo para reparar la herida, sino también para reemplazar la extremidad perdida. A continuación, se aplicó la proteína morfogenética ósea 2 (BMP2), que transmite las señales al blastema para que comience a formarse, además del trabajo preparatorio realizado por el FGF2.
El tratamiento con doble proteína fue suficiente para regenerar huesos, tendones, ligamentos y estructuras articulares —es decir, los elementos esqueléticos y de tejido conectivo del dedo que faltaba— tras docenas de intentos en pruebas realizadas en ratones. Si bien los dígitos de reemplazo a veces estaban deformados o eran demasiado pequeños, todas las partes esenciales estaban presentes.
Lo interesante de este enfoque es que resulta inusual en el campo más amplio de la medicina regenerativa. Normalmente, la atención se centra en la aplicación de células madre frescas, que posteriormente pueden transformarse en una gran variedad de tipos celulares.
“No es necesario obtener células madre y reintroducirlas”, explica Muneoka sobre el método que utiliza su equipo.
“Ya están ahí; solo necesitas aprender a conseguir que se comporten como tú quieres”.
El nuevo estudio se basa en investigaciones anteriores del mismo laboratorio, que utilizaron un enfoque similar de señalización de proteínas. Sin embargo, en esos experimentos anteriores no se utilizó FGF2, no se formó blastema y sólo se regeneró una parte de la extremidad faltante.
“Esto cambia nuestra forma de pensar sobre lo que es posible”, explica el coautor y fisiólogo veterinario Larry Suva.
“Una vez que se demuestra que la regeneración puede activarse, se abre la puerta a plantear preguntas completamente nuevas”.
Sin duda, no es la primera vez que los científicos sospechan que nuestros poderes regenerativos podrían estar ocultos en nuestro interior, en lugar de estar completamente ausentes. Por supuesto, si se logran encontrar y mejorar, las implicaciones para los tratamientos médicos serán enormes.
Queda mucho trabajo por hacer antes de que este nuevo enfoque pueda probarse en humanos, incluyendo un análisis más detallado de los mecanismos de regeneración y la producción de extremidades que se parezcan más a las que se han perdido.
Dado que la BMP2 ya está aprobada para su uso en cirugía reconstructiva y la FGF2 está en camino de obtener el mismo estatus, también podría haber beneficios más inmediatos: mejorar la reparación de heridas y reducir las cicatrices, incluso si no hay una regeneración real.
“La razón por la que algunos animales pueden regenerarse y otros, en particular los humanos, no, es una gran incógnita que se ha planteado desde Aristóteles”, afirma Muneoka.
“He dedicado mi carrera a intentar comprender eso”.
La investigación ha sido publicada en Nature Communications.
Fuente: Live Science.