A primera vista, parecía un error genético, tan grave que debería haber dejado inválido al animal. Pero, en cambio, contribuyó a convertir a los caballos en corredores de fondo naturales.
Investigadores que estudiaban el ADN de casi 200 especies de mamíferos notaron algo extraño en el genoma de los caballos: una mutación en un gen que debería haber inhibido un proceso celular clave. El gen, KEAP1, es vital para defender a las células del estrés químico causado por los altos niveles de metabolismo del oxígeno. Sin embargo, de alguna manera, los caballos no solo sobrevivían con este gen dañado, sino que prosperaban.
Un pacto con el diablo, perfeccionado
“Para generar energía, hicimos un pacto con el diablo”, declaró a NPR Gianni Castiglione, biólogo evolutivo de la Universidad de Vanderbilt. “Para, básicamente, tener un fuego de combustión lenta en nuestras células”.
Ese fuego impulsa nuestras vidas, convirtiendo el oxígeno en energía en forma de ATP. Pero también produce especies reactivas de oxígeno (ERO), moléculas tóxicas que pueden dañar el ADN, las proteínas y las membranas celulares. Para la mayoría de los animales, esto presenta una desventaja: producen demasiada energía y las células se ven sobrecargadas por el daño. Pero los caballos, al parecer, encontraron una solución.
“Los caballos pueden hacer que este fuego arda aún más y que el daño sea incluso menor que en una especie como la humana”, dijo Castiglione.
Publicado en Science, el nuevo estudio revela cómo una rara mutación genética en el gen KEAP1 permite a las células equinas potenciar su producción de energía, a la vez que refuerzan sus defensas innatas contra el estrés. Esta capacidad podría explicar cómo los caballos evolucionaron, pasando de ser habitantes del bosque del tamaño de un perro, a atletas musculosos que dominan las carreras de resistencia, cruzan desiertos y escapan de los depredadores con facilidad.
Rompiendo las reglas genéticas

El gen KEAP1 normalmente codifica una proteína que actúa como un portero molecular. Se une a otra proteína, NRF2, manteniéndola fuera de la sala de control celular (el núcleo), donde podría activar genes de respuesta al estrés.
Cuando los niveles de ROS se disparan, la proteína KEAP1 libera a NRF2, lo que le permite entrar al núcleo y activar las defensas antioxidantes. Se trata de un equilibrio delicado que, si se altera, puede provocar inflamación o muerte celular.
En el ADN del caballo, los investigadores encontraron lo que parecía un error catastrófico: un codón de parada prematuro, una secuencia genética de tres letras (UGA) que le dice a la maquinaria de producción de proteínas de la célula que deje de traducir el gen.
“Ese tipo de mutación mata a los ratones”, dijo Castiglione. “Pensamos: ¡Vaya! ¿Cómo se comportan los caballos con esto?”.
En la mayoría de los casos, un codón de terminación cerca del inicio de un gen implicaría que no se produce ninguna proteína funcional. Es como detener el ensamblaje de un coche tras instalar un solo tornillo. El gen KEAP1 codifica una proteína de más de 600 aminoácidos; la mutación en caballos debería haberla dejado con solo 14.
Pero cuando Castiglione y sus colegas examinaron células de caballo, descubrieron algo sorprendente: KEAP1 todavía se estaba produciendo, estaba completamente formado y era funcional.
“Un día, se me encendió la luz”, recordó Castiglione en una entrevista con Science.
En lugar de obedecer la señal de parada, las células de los caballos la ignoraron. Recodificaron el codón de parada UGA como cisteína, un aminoácido con propiedades químicas especiales. Este raro fenómeno, llamado lectura del codón de parada, se había observado principalmente en virus. En los caballos, operaba en el corazón mismo de un sistema crítico de regulación del estrés.
Convertir un error genético en una característica
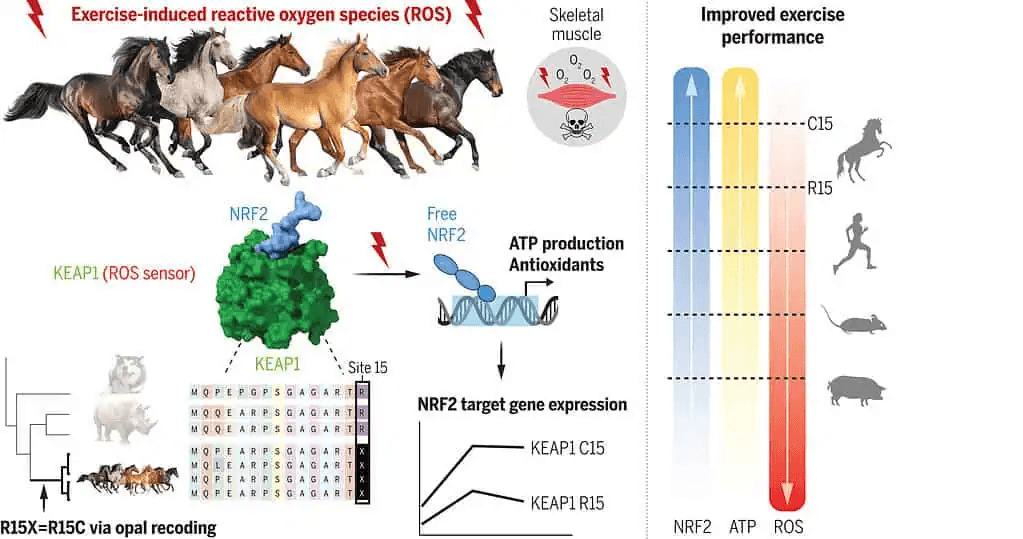
“Debería haber causado una pérdida catastrófica de la función de esta proteína”, dijo Samantha Brooks, experta en genética equina de la Universidad de Florida. “Pero, en cambio, los ancestros de estas especies lograron, de alguna manera, convertir ese limón en limonada”.
La solución genética alternativa no sólo mantiene el sistema funcionando, sino que lo potencia. Añadir cisteína adicional a la proteína KEAP1 la hace más sensible al estrés oxidativo. Esto permite que las células de caballo respondan con mayor rapidez y eficacia a las ROS. Los ensayos metabólicos demostraron que las células musculares de caballo producen cinco veces más ATP que las células de ratón, a la vez que aumentan su respuesta antioxidante en un 200%.
“Esto les proporciona los medios bioquímicos para correr rápido y largas distancias”, dijo Elia Duh, científica clínica de la Universidad Johns Hopkins y coautora principal del estudio.
Los científicos utilizaron CRISPR, espectrometría de masas y ensayos metabólicos en células humanas y equinas. Encontraron dos proteínas, conocidas como SBP2 y eEFSec, que presentan mutaciones únicas en el género equino (Equus). Estas proteínas parecen haber evolucionado en paralelo con cambios en el propio gen KEAP1. Juntos, la mutación genética y sus agentes secundarios actúan como un GPS celular que redirige el tráfico para evitar un obstáculo.
Implicaciones evolutivas y biomédicas
Esta inusual mutación aparece en todos los miembros vivos de Equus, incluyendo burros y cebras. Esto sugiere que el cambio ocurrió en las primeras etapas del linaje y podría haber desempeñado un papel fundamental en la evolución de la notable resistencia del grupo.
“Una vez que descubrieron cómo correr, pudieron ocupar todo tipo de nichos ecológicos”, dijo Castiglione.
José Calbet, un fisiólogo del ejercicio que no participó en el estudio, calificó el trabajo de “excepcional” y elogió su enfoque molecular detallado para un rompecabezas evolutivo de larga data. Más allá de los conocimientos evolutivos, los hallazgos también podrían aportar información a la medicina.
Aproximadamente el 10% de las enfermedades genéticas humanas son causadas por codones de terminación prematuros que truncan proteínas importantes. Si los investigadores logran descifrar cómo los caballos recodifican estas señales de terminación, esto podría ofrecer nuevos enfoques de terapia génica para afecciones como la fibrosis quística o la distrofia muscular.
“La identificación de este evento de recodificación del UGA evolutivamente significativo representa un hallazgo potencialmente fundamental”, dijo Hozumi Motohashi, biólogo de la Universidad de Tohoku.
Para Duh, las implicaciones van más allá de los caballos.
“Al observar lo que la evolución ha descubierto, sabemos que esta es una estrategia viable”, dijo. “La naturaleza nos muestra un camino que algún día podríamos usar para sanar”.
Fuente: ZME Science.

